La rouille sur une poutre métallique
Acier au sec, dure des siècles ; acier mouillé, fini feuilleté.
Visite de diagnostic ordinaire.
On s’arrête devant une poutre et un intervenant s’alarme :
« Oh là ! Vous avez vu cette poutre ?! Elle est toute rouillée, il faut la changer ! »
Il nous est plusieurs fois arrivé d’entendre ce type de réaction.

Photographie d’une poutre métallique légèrement corrodée dans un atelier ancien lors d'un diagnostic Réparabat.
Dans la conscience collective, la rouille est synonyme de danger, de perte de portance, voire d’effondrement futur.
Mais ici, on vous le dit : la poutre est en parfait état.
Pour comprendre la corrosion, retenez une phrase simple :
« La nature privilégie toujours l’état qui demande le moins d’énergie pour exister, car c’est l’état le plus stable. »
Si je place une poutre métallique dans mon salon, sans protection, l’acier s’oxyde légèrement, car nous vivons dans un milieu oxydant : l’air.
Une mince couche de corrosion se forme… et c’est tout.
Pourquoi ?
Parce qu’en milieu sec, l’acier se corrode extrêmement lentement, son état est relativement stable. La vitesse de corrosion est si faible qu’elle n’est pas significative à l’échelle d’une vie humaine.
• En milieu humide, on observe environ 1 à 10 µm/an.
• En milieu sec, on peut estimer environ 0,1 µm/an.
Sur 100 ans :
0,1 µm × 100 = 10 µm
Soit 0,01 mm.
Schéma simplifié de l'influence du milieu sur la corrosion des poutres métalliques en batî ancien.
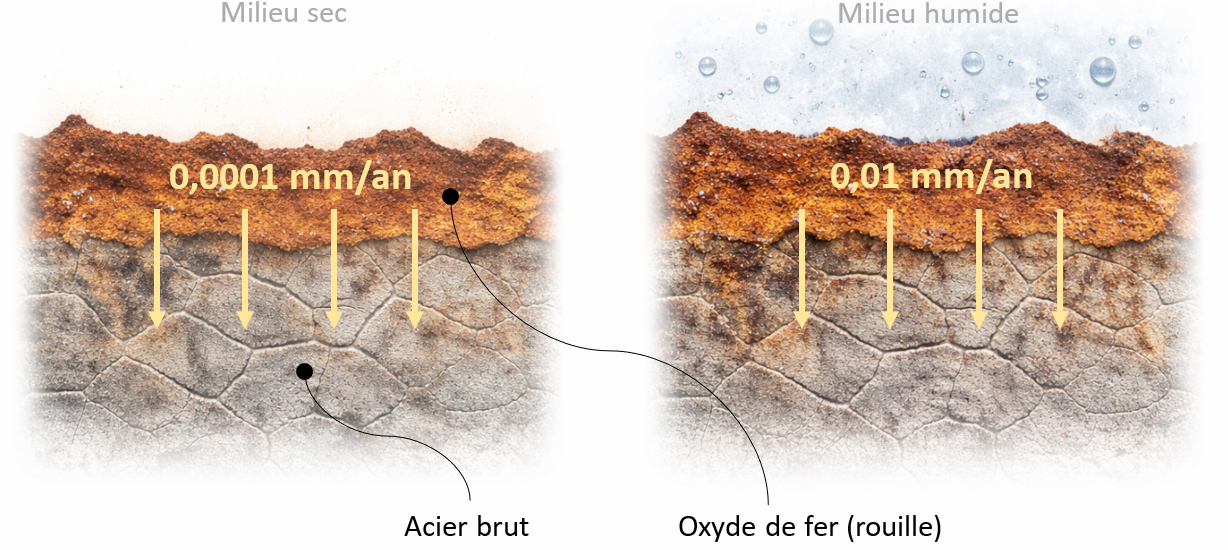
Autrement dit, la corrosion est quasi nulle.
Mais il suffit d’un troisième acteur pour que la situation change : l’eau.
Pourquoi l’eau ?
Parce qu’elle permet la circulation des charges électriques. Dans un milieu Eau + Acier + Oxygène, des déséquilibres électrochimiques apparaissent.
Un courant électrique microscopique circule.
• Oxygène : très électronégatif, il cherche à être plus stable en gagnant des électrons.
• Acier : relativement stable en milieu sec, la réaction est extrêmement lente, mais sa capacité à retenir ses électrons est faible face à la force d’arrachement de l’oxygène.
• Eau : permet la circulation des charges électriques.
Résultat : l’oxygène arrache des électrons à l’acier brut, formant de l’oxyde de fer, qu’on appelle rouille, matériau mécaniquement faible.
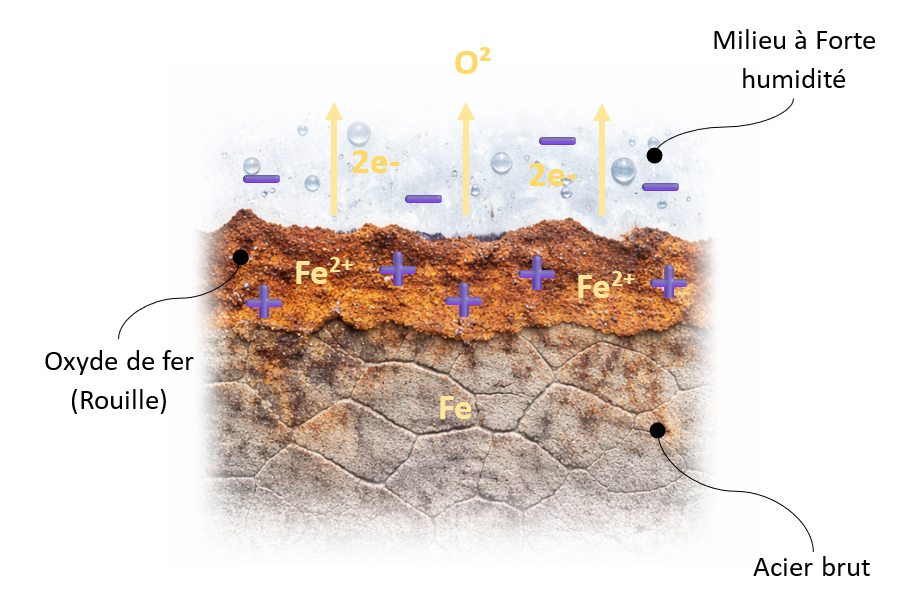
Schéma simplifié sur le mécanisme électrochimique de formation de la rouille sur une poutre en acier
Les trois points essentielles à retenir :
